ひとつのプラットフォームが持つ無限の可能性
RASTRUM™ は、次世代の創薬や医学・生物学研究のために、3D細胞培養モデルを提供します。
最適化された硬さ(組織スティッフネス)、細胞外マトリクスタンパク質や足場ペプチドの含有を組み合わせた機能的なマトリクス構造により、従来の前臨床モデルでは不可能であったようなin vivo組織微小環境を、研究者は再現することができます。
この自動化され、自動化され、再現性の高いプラットフォームにより、研究者は複雑な生物学を確実にモデル化でき、新しい治療標的の発見や、薬剤化合物のスクリーニングへ利用することができます。
RASTRUM™ 3D細胞培養モデル

Imaging Model(小型の単一マトリクス)
薄型の単一マトリクスの3D細胞培養モデル
∙ 蛍光免疫染色イメージング
∙ 化合物スクリーニング
∙ 生化学的なアッセイ
∙ ハイコンテンツイメージングのための薄型モデル
∙ 使用する細胞量を最小限に

Large Plug Model(大型の単一マトリクス)
ウェル底一面にゲルが敷かれた単一マトリクスの3D細胞培養モデル
∙ DNA, RNA やタンパク質の解析
∙ フローサイトメトリー
∙ オミックス解析
∙ 細胞数が必要なアッセイ
∙ ハイコンテンツイメージングも可能な薄型(イメージングモデルと同じ高さ)

Hight Throughput (HTP) Model
384ウェルプレートのためにデザインされた単一マトリクスの3D細胞培養モデル
∙ 化合物スクリーニング
∙ ハイコンテンツスクリーニング
∙ 生化学的アッセイ
∙ 高いスループットが必要なアッセイ

Triple Matrix Model(三つのマトリクス)
積層構造を再現するためにデザイン(垂直方向への積層を水平方向に展開)
∙ 細胞遊走アッセイや浸潤アッセイ
∙ 組織構造(積層構造)の再現
∙ 細胞間シグナル伝達や相互作用
∙ 細胞間のシグナル伝達や相互作用のイメージングが容易
∙ 組織構造を模倣した3D細胞培養モデル

Dual Matrix Model(二つのマトリクス)
積層構造を再現するためにデザイン(垂直方向への積層を水平方向に展開)
∙ 細胞遊走アッセイや浸潤アッセイ
∙ 組織構造(積層構造)の再現
∙ 細胞間シグナル伝達や相互作用
∙ 細胞間のシグナル伝達や相互作用のイメージングが容易
∙ 組織構造を模倣した3D細胞培養モデル
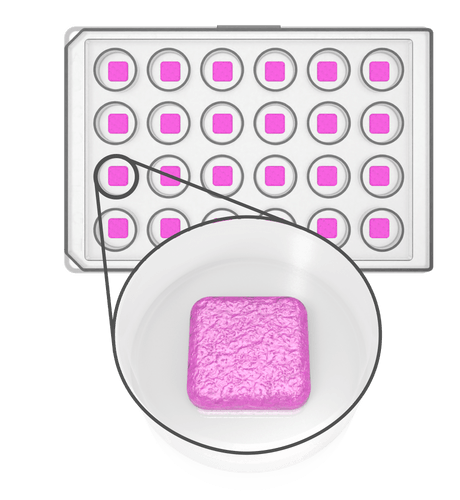
Removable Model
24ウェルプレートのカバースリップに印刷された取り外し可能モデル
∙ 細胞移植
∙ 免疫組織化学染色
∙ 空間生物学
∙ 顕微鏡でのイメージングのための取り外しが容易
∙ 包埋や切片作製
私たちの関心分野
腫瘍免疫
腫瘍免疫学は、がんと闘うために免疫系を活用する研究であり、がん治療に革命をもたらしました。腫瘍免疫学研究を加速させるためには、腫瘍微小環境を正確に再現する、生理学的に適切なin vitroアッセイの構築が不可欠です。RASTRUM™は、腫瘍細胞と免疫細胞の相互作用の研究や、生理学的に適切な状況での免疫療法の評価を可能にします。
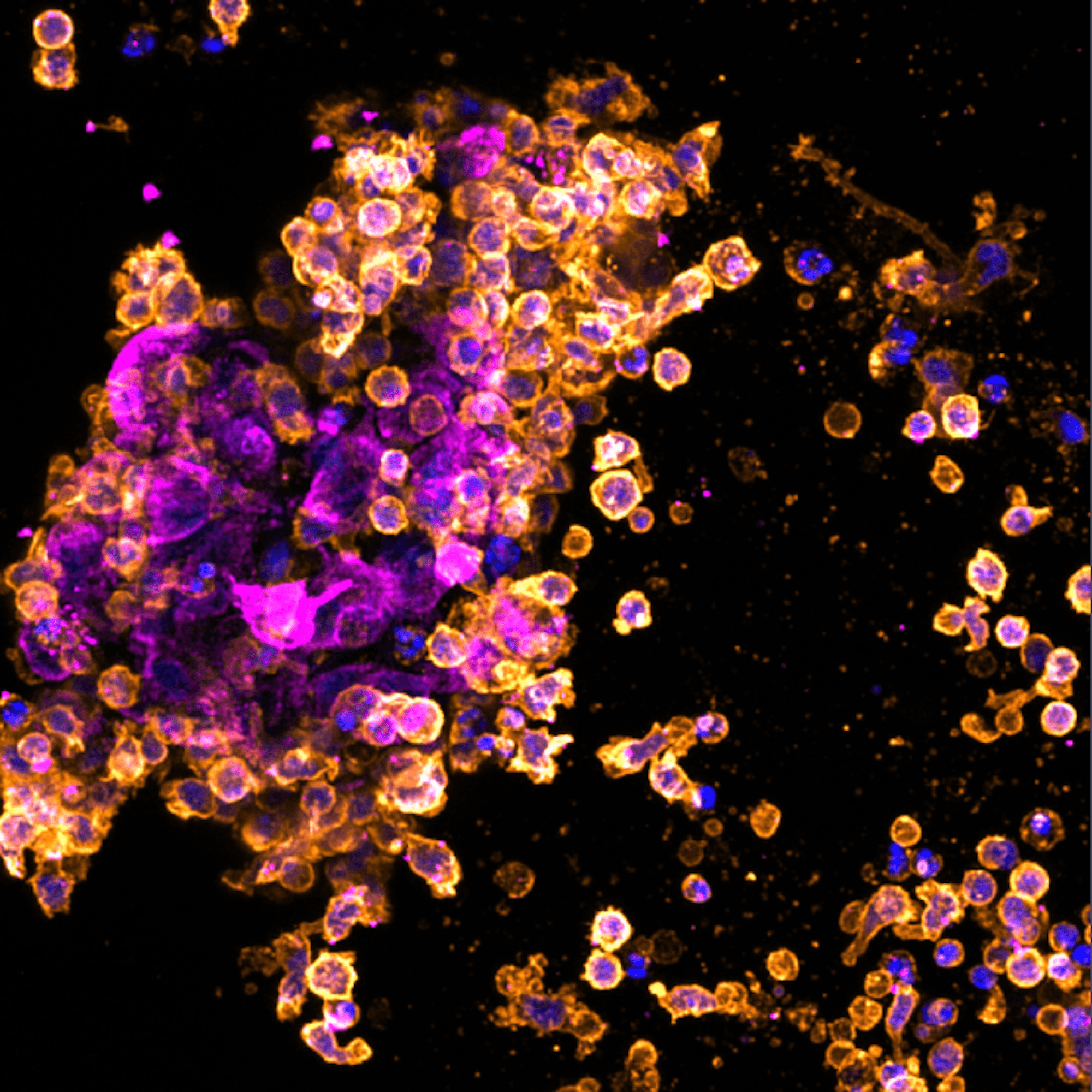
脳、iPS細胞
人工多能性幹細胞(iPSC)は、神経変性疾患の研究や創薬に大きな可能性をもたらすと期待されています。iPS細胞は様々なタイプの中枢神経系(CNS)細胞に分化することができ、アルツハイマー病、パーキンソン病、ハンチントン病などの疾患の研究に役立つと考えられています。生理学的に適切なin vitro中枢神経系モデルを作成することは、疾患を理解し、治療方法を検証するために不可欠です。これらのモデルは細胞レベルで疾患の進行を明らかにし、特異な表現型や治療標的の特定を助けます。この研究の成功の鍵は、複数の機能的なiPSC由来CNS細胞を使用し、複雑な神経変性疾患構造を再現できるかどうかにかかっています。RASTRUM™は、複数のiPSC由来CNS細胞を用い、生体への適合性があり、かつ複雑な微小環境を持つ神経細胞モデルの作製を可能にします。

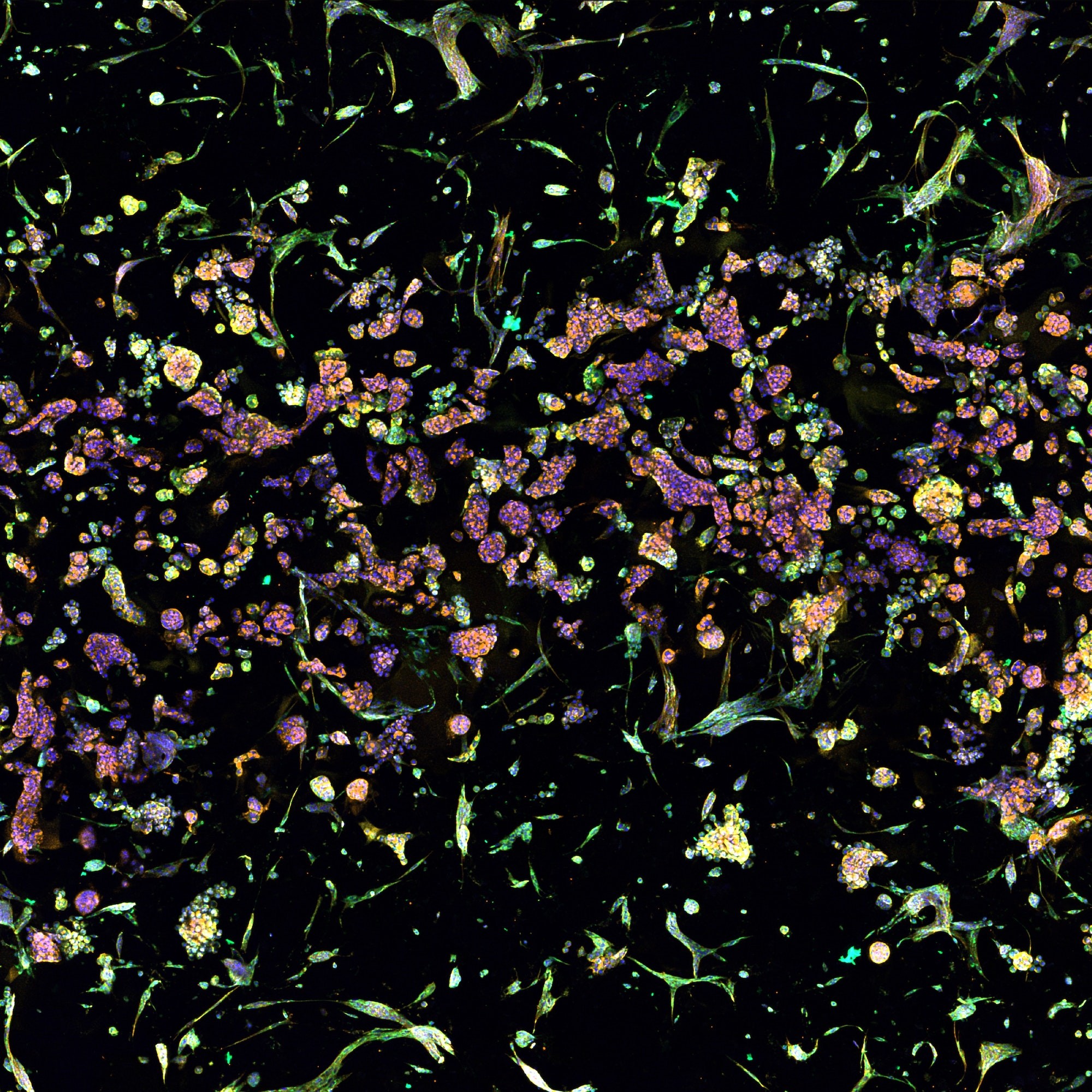
線維芽細胞
線維芽細胞は、組織構造の維持、創傷治癒、免疫反応において重要な役割を果たしています。線維芽細胞の挙動と細胞間の相互作用を理解することは、癌、線維症、炎症性疾患など様々な疾患の背後にあるメカニズムを解明するための鍵となり得ます。線維芽細胞研究から得られる洞察は、革新的な治療法の開発につながる可能性があり、医学・生物学研究において不可欠な研究分野となっています。RASTRUM™では、硬さや生体機能を持つマトリクスを調整可能なため、生理学的に適切な線維芽細胞の微小環境を細胞に与えることができ、生体に類似した環境でのハイスループットな標的探索と表現型スクリーニングが可能となります。
肝臓
肝毒性は、創薬における重要な課題であり、臨床試験の中止や失敗の一因でもあります。創薬の前臨床段階において、動物モデルはヒトの薬剤肝障害(DILI)を予測するには信頼性に欠け、現行の3D細胞培養モデルは、拡張性の低さ、作業の煩雑さ、といった創薬ワークフローの適合性に課題を抱えています。このため、DILIのためのin vitroヒト細胞モデルが必要とされています。RASTRUM™によって作製される3D肝細胞培養モデルは、DILI研究への応用が可能です。
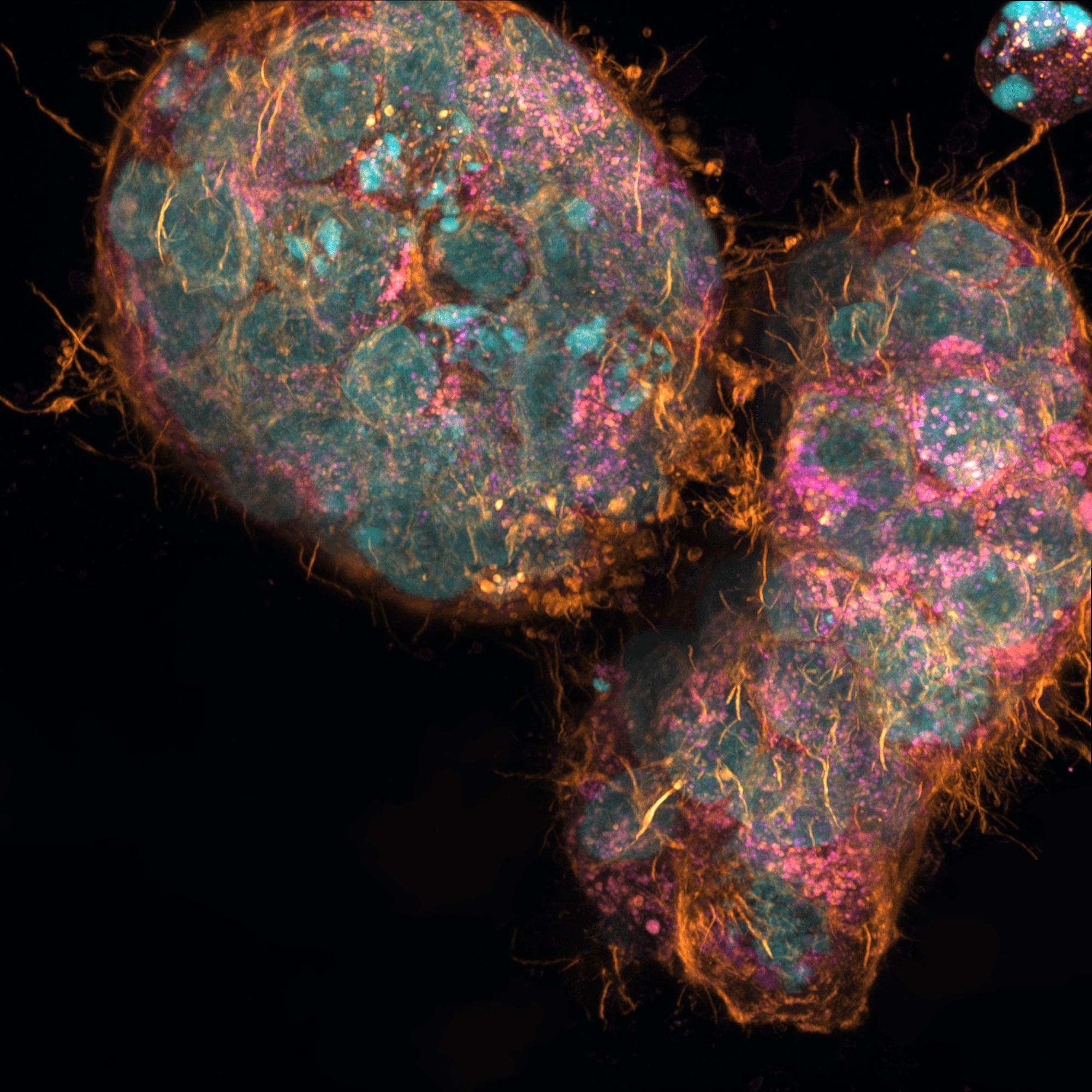
質問はありませんか?私たちのサイエンティストがお答えいたします。